
近日,美國FDA發布了最新的《醫療器械製造商檢查合規計劃手冊》(CP7382.850),全麵更新了對醫療器械生產企業的監管框架。新規將於2026年2月2日正式生效,旨在確保醫療器械全生命周期的安全性與有效性。下述核心要點,值得所有從業者重點關注:
一、新規核心監管要求
🔍 核心轉變:基於風險的檢查
FDA將采用全新的“基於風險”策略安排檢查優先級。高風險產品(如植入式、生命支持類器械等)、存在不良合規記錄(高召回率、MDR報告頻發)的企業以及首次受檢的三類器械製造商,將成為重點對象。
📋 兩大檢查模型,針對性更強
手冊明確劃分兩類標準化檢查流程:“模型1”適用於常規或後續檢查,需全麵評估質量體係各領域;“模型2”適用於首次或上市前檢查,聚焦核心特定要素。實現檢查流程精準匹配、高效落地。
🔄 質量體係與國際接軌
FDA正式將國際標準 ISO 13485:2016 納入質量管理體係法規(QMSR),重點強調企業質量文化建設與流程整合要求,明確企業需從設計開發、生產製造到售後服務全流程,均需嚴格符合風險管理要求。
⚡ 聚焦高風險與特殊環節
上市前批準(PMA):三類高風險器械需通過嚴苛審批流程,檢查重點聚焦工藝驗證與設計開發全流程合規性。
上市後監督:FDA將對已獲批的高風險器械開展定期檢查,同步重點關注網絡安全、輻射安全等新興風險領域。
特殊主體:二手器械再製造商、一次性器械再處理商等主體被視同製造商,正式納入統一監管範圍。
📈 監管後手:從警告到司法行動
FDA按違規嚴重程度明確梯度化處置措施,涵蓋警告信、產品扣押、禁令直至刑事起訴等;對屢教不改的企業,將要求其聘請外部審計機構核查,並提交年度合規認證報告。
二、 企業應對新規的行動指南:六大舉措即刻落地
🛠️麵對已經生效的新規,醫療器械企業需快速啟動合規整改工作,從體係梳理到實操落地全方位推進,具體行動舉措如下:
開展差距分析
係統對比現有質量體係與QMSR新規以及ISO 13485:2016標準的所有要求,找出差距。已經獲得ISO 13485:2016認證的企業會相對輕鬆,但仍需關注FDA的特定要求。
升級質量管理體係文件
依據差距分析結果,更新質量手冊、程序文件等核心文件,確保反映新規的所有變化,特別是術語和風險管理要求的更新。
強化風險管理
確保風險管理活動覆蓋產品全生命周期,從設計開發、生產到上市後監督,並符合ISO 14971標準。
準備關鍵文件
梳理並確保設計曆史文件(DHF)、器械主記錄(DMR)、器械曆史記錄(DHR) 以及CAPA(糾正與預防措施) 記錄的完整性、準確性與可追溯性。
內部培訓與溝通
針對全體員工開展新規專項培訓,重點強化高層管理者、質量相關崗位人員的合規認知,確保全員理解並落地基於風險的管理思維與新流程要求。
模擬檢查與自查
可以參照FDA新的檢查程序手冊進行內部模擬審計,熟悉可能的新檢查流程和提問方式,提前發現潛在問題。
三、一圖看懂:檢查內容架構
無論是模式1還是模式2,檢查內容都圍繞以下6+4結構展開:
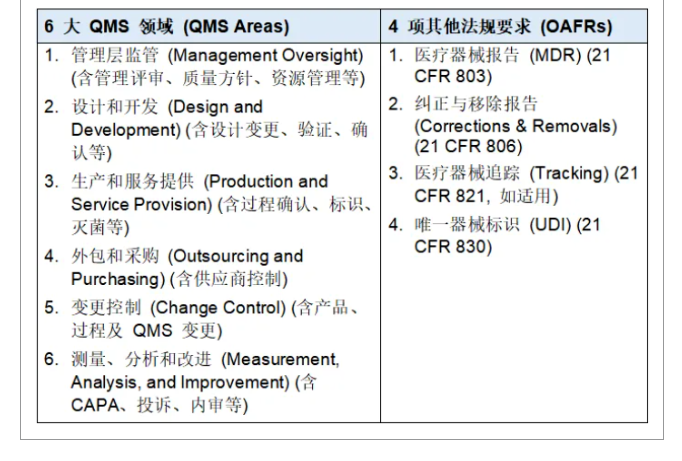
本手冊正式取代了舊版文件,標誌著FDA對醫療器械的監管邁入更係統、更嚴格、更國際化的全新階段。相關企業應盡早熟悉新規,完善自身質量體係,以應對即將到來的檢查挑戰。
為助力企業精準拆解新規要點、高效落地合規整改動作,金飛鷹藥械谘詢技術服務集團特推出FDA新規解讀與合規實操專項培訓,培訓時間定於2月26日下午3點,感興趣的朋友記得鎖定本次的精華課程,精準把握合規方向、築牢體係建設根基!
信息來源:FDA 排版整理:金飛鷹藥械



